on Heidelberg Pharma AG (ETR:HPHA)
Heidelberg Pharma fait progresser son candidat ADC HDP-101 vers la phase II des essais cliniques.
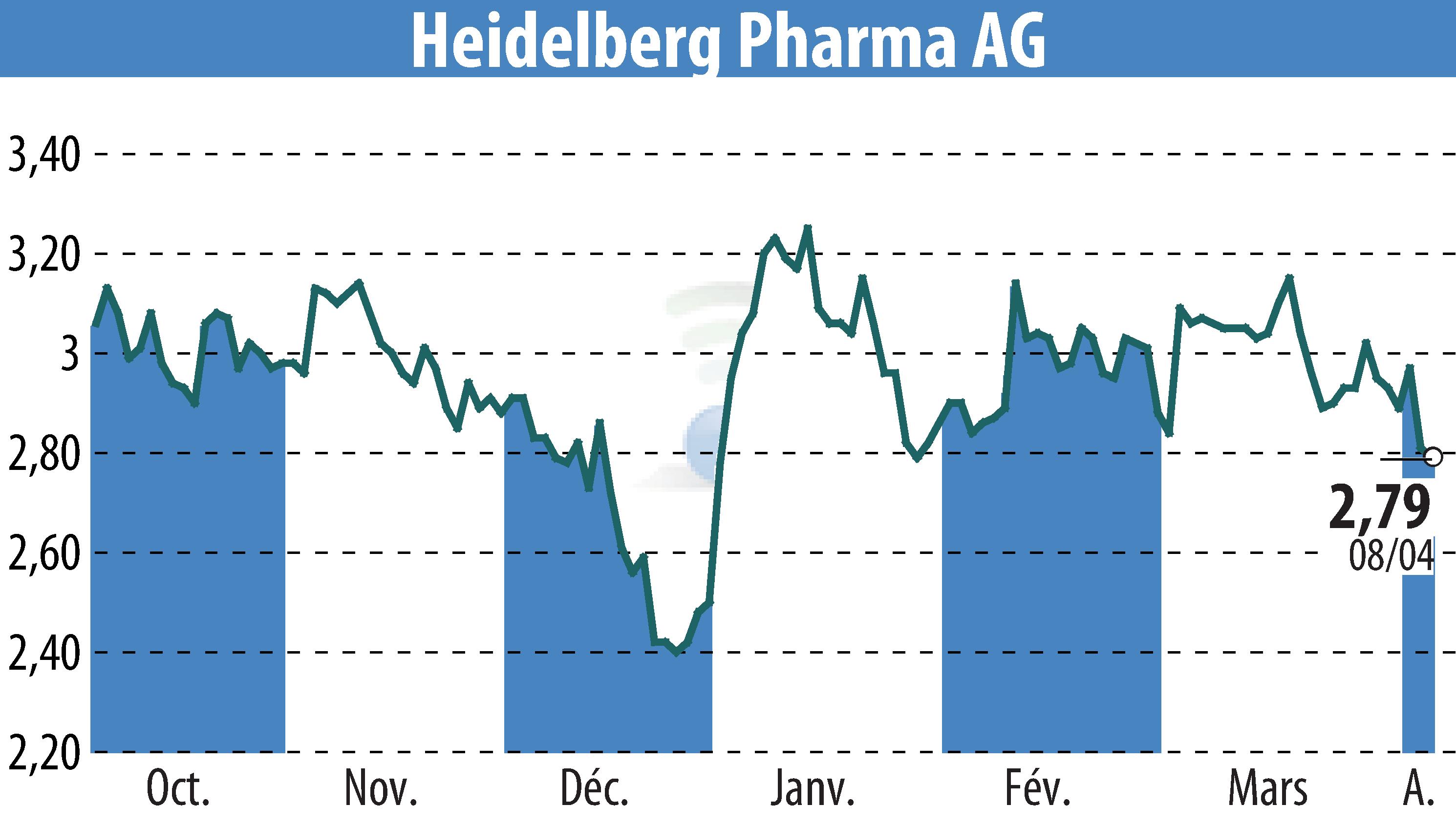
Heidelberg Pharma AG a annoncé une avancée majeure dans son essai clinique de l'ADC candidat HDP-101, avec la détermination de la dose recommandée pour la phase II (RP2D). L'essai de phase I mené avec le pamlectabart tismanitin a démontré un profil de sécurité et de tolérance prometteur, justifiant cette décision. Après avoir examiné les données de sécurité et de pharmacocinétique, le comité d'évaluation de la sécurité de l'étude a approuvé le passage à la phase IIa.
L'essai de phase IIa à venir vise à évaluer plus précisément l'activité antitumorale du pamlectabart tismanitin chez les patients atteints de myélome multiple en rechute ou réfractaire. Le recrutement des patients devrait débuter dans les prochaines semaines dans les centres d'étude existants, avec une cohorte prévue de 30 patients. Les données relatives à la sécurité et à l'efficacité seront présentées lors d'un prochain congrès scientifique.
L'approche novatrice d'Heidelberg Pharma repose sur l'utilisation d'une technologie ADC à base d'amanitine, faisant du HDP-101 un candidat prometteur dans le traitement du myélome multiple. Ce candidat a déjà obtenu les désignations de procédure accélérée et de médicament orphelin, soulignant ainsi son importance.
R. H.
Copyright © 2026 FinanzWire, all reproduction and representation rights reserved.
Disclaimer: although drawn from the best sources, the information and analyzes disseminated by FinanzWire are provided for informational purposes only and in no way constitute an incentive to take a position on the financial markets.
Click here to consult the press release on which this article is based
See all Heidelberg Pharma AG news
